Introduire des produits thérapeutiques dans le cerveau
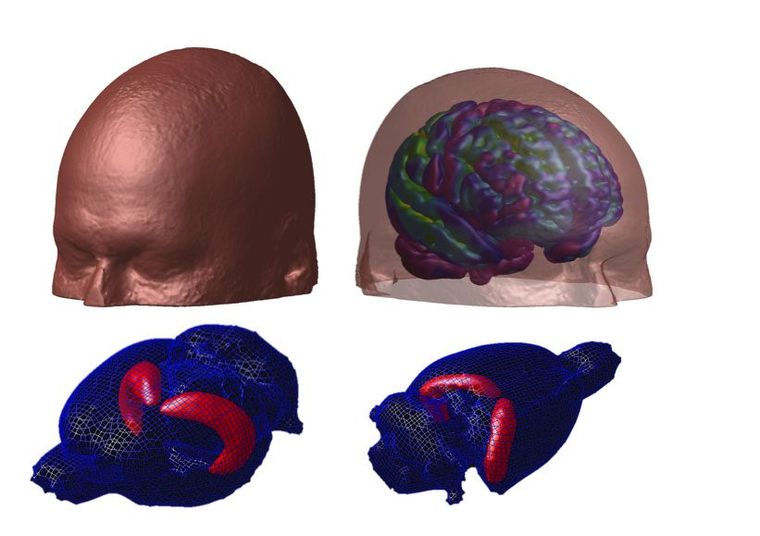
Ces images ont été créées par le laboratoire de la Dre RosaNeto à l'Hôpital Douglas de l'Université McGill et montrent la fusion entre l'anatomie du cerveau et le dépôt d'amyloïde dans le cerveau humain vivant (rangée du haut) et dans celui du rat (rangée du bas).
Aucune molécule modifiant la maladie d'Alzheimer n'est actuellement sur le marché ou utilisée. Il s'agit de l'un des plus grands besoins médicaux non satisfaits dans le domaine des neurosciences. Si aucun remède n'est trouvé d'ici 2038, le coût total des soins devrait atteindre 153 milliards de dollars rien qu'au Canada. L'administration de médicaments à des cibles cérébrales est considérablement entravée par une couche protectrice spéciale, appelée barrière hémato-encéphalique, qui est conçue pour empêcher les toxines et tout ce qui est potentiellement nocif d'atteindre le cerveau, mais qui empêche également des médicaments qui pourraient sauver des vies d'atteindre le cerveau.
Nathan Yoganathan et son équipe travaillent sur un moyen de résoudre ce problème. Leur objectif est de prendre une molécule modificatrice de la maladie d'Alzheimer qui se lie aux protéines amyloïdes toxiques et de la faire passer en douce à travers la barrière hémato-encéphalique en l'attachant à une autre molécule capable de la franchir. C'est ce qu'on appelle la méthode du cheval de Troie, et si l'équipe réussit, ce serait la première fois que l'on y parvient chez l'homme. Le projet est le fruit d'une collaboration entre des universités, des organisations à but non lucratif et des petites et moyennes entreprises. L'équipe multidisciplinaire et multi-institutionnelle de tout le pays teste l'efficacité d'une molécule modificatrice de la maladie d'Alzheimer de Kalgene couplée à une molécule porteuse, toutes deux développées par le Conseil national de recherches et concédées sous licence à Kalgene. L'Institut neurologique de Montréal et CIMTEC sont également impliqués, et leur expertise en imagerie et en diagnostic permettra de mesurer si la molécule conjuguée est capable de traverser la barrière hémato-encéphalique chez l'homme et de se lier efficacement à l'amyloïde toxique.
Les objectifs du projet sont doubles : Démontrer avec succès que cette méthode du cheval de Troie, qui a fait ses preuves dans les modèles précliniques, fonctionnera également pour délivrer le peptide dans le cerveau humain et que le médicament est sûr dans les essais cliniques de phase 1. Ces deux objectifs ont déjà été atteints dans les études précliniques, qui ont également démontré l'efficacité du peptide dans l'élimination de la bêta-amyloïde. L'équipe a déjà réalisé des progrès significatifs. En étroite collaboration avec Kalgene, le laboratoire de neuro-imagerie translationnelle (Centre de recherche McGill pour les études sur le vieillissement, Université McGill) a démontré la perméabilité de la barrière hémato-encéphalique, l'engagement de la cible et l'efficacité du médicament in vivo en utilisant des méthodes d'imagerie dans des modèles transgéniques. Ces résultats passionnants seront annoncés lors de la conférence internationale de l'Alzheimer's Association, qui se tiendra à Londres en juillet 2017. Début 2018, KalGene lancera le premier essai clinique chez l'homme, qui sera dirigé par Pedro Rosa-Neto, Serge Gauthier et Angela Genge de l'Université McGill. En outre, ce projet permet de former un grand nombre de professionnels hautement qualifiés dans les domaines du développement avancé de médicaments et des essais cliniques.
Si l'équipe parvient à démontrer que ce médicament modifiant la maladie d'Alzheimer peut être administré en toute sécurité dans le cerveau, cela pourrait également accélérer le développement de thérapies pour d'autres affections cérébrales.
"Cette subvention a servi de catalyseur pour rassembler les universitaires, les cliniciens et les entreprises du Canada afin d'utiliser les actifs canadiens, la propriété intellectuelle canadienne et l'expertise canadienne à tous les niveaux, y compris les cliniciens, pour faire avancer le projet"
Nathan Yoganathan, Ph.D., PDG de Kalgene Pharmaceuticals
